Rakutsükkel
Rakutsükkel ehk raku jagunemistsükkel on raku elukäik pooldumisest pooldumiseni.
Rakutsükkel koosneb reast sündmustest, mis viivad raku jagunemise ja kahekordistumiseni.
Rakutuuma omavate ehk eukarüootsete rakkude rakutsükkel jaotatakse kolmeks osaks:
- interfaas – toimub raku kasvamine, mitoosiks vajalike toitainete kogumine ja DNA kahekordistamine;
- mitoos – tulemuseks on raku jagunemine kaheks erinevaks rakuks, mida kutsutakse tütarrakkudeks;
- tsütokinees – toimub raku lõplik jagunemine.
Rakkude jagunemine toimub hulkraksetel organismidel kasvuperioodil. Kogu elu vältel toimub mitmete kehakomponentide – näiteks karvade, naha, vererakkude ja mõnede siseelundite – kudede uuenemine rakkude pooldumise teel.
Rakutsükli faasid muuda
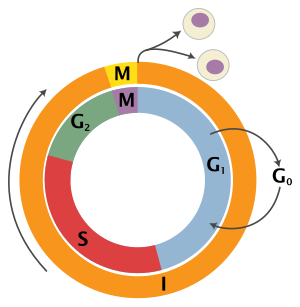
Rakutsükkel koosneb neljast eristatavast faasist: G1-faas, S-faas (süntees), G2-faas (need kolm kokku moodustavad interfaasi) ja M-faas (mitoos). M-faas ise koosneb kahest omavahel tihedalt ühendatud protsessist: mitoosist, kus jaotatakse raku kromosoomid kahe tütarraku vahel, ning tsütokineesist, kus jaotatakse raku tsütoplasma kaheks ja moodustub kaks eraldi rakku.
Ükski faas ei käivitu enne, kui eelmine on täielikult lõpuni viidud. Rakud, mis ajutiselt või pöörduvalt on lõpetanud jagunemise, on puhkefaasis, mida nimetatakse G0-faasiks.
Pärast raku jagunemist alustab iga tütarrakk uue rakutsükliga. Kuigi interfaasi erinevad staadiumid ei ole tavaliselt morfoloogiliselt eristatavad, on igal faasil eriliselt spetsialiseerunud biokeemilised protsessid, mis valmistavad rakku ette jagunemise alguseks.
Puhkefaas (G0-faas) muuda
Hulkraksetes organismides väljuvad enamik diferentseerunud rakke rakutsüklist, jäädes G0-faasi pikaks ajaks või mõnel juhul kogu eluks (südamelihase rakud, närvirakud). Kui rakutsüklisse uuestisisenemist enam kunagi ei toimu, nimetatakse neid rakke postmitootilisteks rakkudeks. Teatud kasvufaktorite mõjul võib aga osa G0-faasis olevatest rakkudest liikuda tagasi rakutsüklisse, sisenedes S-faasi.
Ka DNA kahjustus või DNA lagundamine võivad olla raku püsivalt G0-faasi jäämise põhjuseks, sel juhul on see biokeemiline alternatiiv raku apoptoosi suunamisele. Kui rakutsüklit DNA kahjustuste puhul ei peatata, võib see põhjustada vähki.[1]
Interfaas muuda
Enne, kui rakk saab hakata jagunema, on tal vaja koguda toitaineid. Kõik ettevalmistused jagunemiseks tehakse interfaasi kolme alafaasi (G1, S, ja G2) jooksul. Kuna raku jagunemine toimub tsükliliselt, eelneb interfaasile eelmise rakutsükli mitoos ja tsütokinees. Interfaas on ka tuntud kui ettevalmistav faas, tuuma jagunemist seal ei toimu.
G1-faas muuda
Esimest interfaasi alafaasi M-faasi lõpust kuni S-faasi alguseni kutsutakse G1-faasiks (G viitab ingliskeelsele sõnale gap, mis tähendab tühimikku, lünka). G1 kutsutakse ka kasvufaasiks, kuna selle faasi jooksul raku biosünteetiline aktiivsus kasvab järsult, eriti võrreldes eelneva M-faasiga. G1-faasis toimub erinevate ensüümide süntees, mida läheb vaja S-faasis. Enamasti on need DNA replikatsiooniks vajalikud valgud. G1 kestus varieerub suuresti isegi sama liigi erinevate rakkude puhul.
S-faas muuda
Järgnev S-faas algab siis, kui algab DNA sünteesimine. Selle faasi lõpuks on kõik kromosoomid kahekordistatud, mis tähendab, et igal kromosoomil on kaks õdekromatiidi. RNA transkriptsiooni ja valgusünteesi tase on väga madal, välja arvatud histoonide tootmine, mis toimubki põhiliselt S-faasis.
G2-faas muuda
G2-faas kestab S-faasi lõpust kuni raku mitoosi sisenemiseni. Taas on näha biosünteesi aktiivsuse kasvu, seekord aga toimub mikrotuubulite tootmine, mis on vajalikud mitoosiprotsessi jaoks. Valgusünteesi inhibeerimine G2-faasis takistab raku enneaegset sisenemist mitoosi.
Mitoos (M-faas) muuda
Küllaltki lühike, keeruline ja tugevalt reguleeritud mitoosifaas kujutab endast rakutuuma jagunemist. Sündmuste jada on jaotatud erinevateks faasideks, kus üks faas ei alga enne, kui eelmine on lõpuni viidud. Need faasid on järgmised:
- profaas
- metafaas
- anafaas
- telofaas
- tsütokinees (rangelt võttes ei ole tegelikult mitoosi osa, kuid toimub telofaasiga paralleelselt)
Mitoos on protsess, kus eukarüootse raku tuumas asuvad kromosoomide paarid kondenseeruvad ja nende külge kinnituvad kiud, mis tõmbavad õdekromatiidid lahku raku poolustele. Enamasti järgneb sellele kohe tsütokinees, mis jagab kromosoomid, tsütoplasma, organellid ja rakumembraani võimalikult võrdselt kahe tütarraku vahel. M-faas koosnebki mitoosist ja tsütokineesist, mille koostöö tulemusena jaguneb algne rakk kaheks tütarrakuks, mis on geneetiliselt identsed üksteisele ja ka algsele rakule. M-faas moodustab umbkaudu 10% kogu rakutsüklist.[2]
Kuna tsütokinees toimub enamasti mitoosiga seotult, kasutatakse sõna "mitoos" samatähenduslikult väljendiga "M-faas", kuigi tegelikult on mitmeid rakke, kus mitoos ja tsütokinees toimuvad eraldi. Nii moodustuvad näiteks mitme tuumaga rakud. Seda nähtust on kõige rohkem seente ja limaseente hulgas, kuid on ka täheldatud teistes organismirühmades. Isegi loomades võivad tsütokinees ja meioos toimuda eraldi, näiteks äädikakärbse embrüonaalse arengu teatud etappides.[3]
Mitoos toimub ainult eukarüootsetes rakkudes, kuid varieerub erinevates liikides. Näiteks loomades toimub "avatud" mitoos, kus tuumaümbris laguneb enne kromosoomide lahknemist. Samal ajal seentes, näiteks Aspergillus nidulans ja Saccharomyces cerevisiae (pärm) viiakse läbi "kinnine" mitoos, kus kromosoomide lahknemisel jääb tuumamembraan terveks. Prokarüootsed rakud, kellel tuum puudub, jagunevad pooldumise teel.[4]
Eukarüootse rakutsükli regulatsioon muuda
Vead mitoosis võivad kas surmata raku apoptoosi teel või põhjustada mutatsioone, mis võivad viia vähi tekkeni. Rakutsükli regulatsioon hõlmab hädavajalikke protsesse raku ellujäämiseks, kaasa arvatud pärilikkusmaterjali kahjustuste tuvastamise ja parandamise kontrollimatu raku jagunemise ennetamisena. Molekulaarsed sündmused, mis kontrollivad rakutsüklit, on järjestatud ja suunatud, mis tähendab, et iga protsess ilmneb järjestikuselt ja rakutsüklit on võimatu ümber pöörata.
Tsükliinide ja CDK-de roll muuda
Kaks klassi regulatoorseid võtmemolekule, tsükliinid ja tsükliinisõltuvad kinaasid (inglise keeles CDK – cyclin dependent kinase), määravad ära raku edasijõudmise läbi rakutsükli[5]. Leland Hartwell, Timothy Hunt ja Paul Nurse võitsid 2001. aastal Nobeli auhinna nende tsentraalsete molekulide avastamise eest[6]. Paljud tsükliine ja CDK-sid kodeerivad geenid on kõikide eukarüootide hulgas konserveerunud, kuid üldiselt omavad keerulisemad elusolendid üksikasjalikumaid rakutsükli kontrollsüsteeme, mis sisaldavad individuaalsemaid komponente. Paljud rakutsükli regulatsioonis osalevad geenid identifitseeriti uurides pärme, eriti pärmi Saccharomyces cerevisiae.
Tsükliinid moodustavad aktiveeritud dimeeri regulatoorse alamühiku ja CDK-d katalüütilise alamühiku. Tsükliinidel ei ole katalüütilist aktiivsust ja CDK-d on inaktiivsed, kui neil pole kõrval tsükliini. Kui CDK-d on tsükliini seondumisega aktiveeritud, viivad nad läbi tavapärast biokeemilist reaktsiooni, fosforüleerimist. See aktiveerib või inaktiveerib sihtmärgiks olevaid valke, mis koordineerivad rakutsükli järgmisse faasi liikumist. CDK-sid ekspresseeritakse rakus pidevalt, aga tsükliine sünteesitakse erinevate molekulaarsete signaalide saamisel spetsiifilistes rakutsükli staadiumites.
Kontrollpunktid muuda
Rakutsükli kontrollpunkte kasutatakse rakus selleks, et jälgida ja reguleerida rakutsükli edenemist[7]. Kontrollpunktid ennetavad rakutsükli edasiliikumist, et tagada vajalike faasispetsiifiliste protsesside läbimine ja DNA kahjustuste parandamine. Rakk ei saa edasi liikuda järgmisse faasi enne, kui kontrollpunkti tingimused ei ole täidetud.
Mitmete kontrollpunktide ülesandeks on tagada see, et kahjustatud või mittetäielikku DNAd ei kantaks edasi tütarrakkudesse. Eksisteerib kaks peamist kontrollpunkti: G1/S ja G2/M. G1/S üleminek on tsükli sagedust piirav koht, mis on tuntud ka kui restriktsiooni punkt. Rakutsükli vastusele DNA kahjustuse jaoks on välja toodud ka alternatiivne mudel, mida tuntakse postreplikatsioonilise kontrollpunktina.
Valk p53 mängib olulist rolli nii G1/S kui ka G2/M kontrollpunktide kontrollmehhanismide käivitamisel.
Roll kasvajate moodustamises muuda
Häired rakutsükli komponentide töös võivad viia kasvajate moodustumiseni. Teatud geenide, näiteks rakutsükli inhibiitorite (valk p53 jt) muteerumisel, võib rakk hakata kontrollimatult jagunema ja moodustada kasvaja. Kasvajarakkude rakutsükkel kestab sama kaua kui normaalsetes rakkudes või isegi kauem. Olenemata sellest on aktiivselt jagunevate rakkude hulk kasvajates palju suurem, võrreldes normaalse koega, kus suur hulk rakke on G0-faasis. Seega toimub rakkude hulga otsene kasv, kuna apoptoosi teel surevate või G0-faasi sisenevate rakkude arv jääb samaks.
Vähiteraapia sihtmärgiks ongi pidevalt rakutsüklit läbivad rakud, kuna nende DNA on raku jagunemise jooksul üsnagi katmata (ei ole seotud kaitsvate DNA-ga seotud proteiinidega nagu tavaliselt) ja seega vastuvõtlik ravimite või kiirituse tekitatavatele kahjustustele. Seda fakti kasutataksegi ära vähiteraapias: märkimisväärne osa kasvajast eemaldatakse kirurgiliselt ning vähirakud, mis alles jäävad, liiguvad kohe G0-faasist G1-faasi. Selle põhjuseks on toitainete, hapniku ja kasvufaktorite järsult kättesaadavaks muutumine. Kiirgus või kemoteraapia aga tapab rakud, mis on värskelt rakutsüklisse sisenenud [8]. Rakud on üldiselt kõige kiirgustundlikumad hilistes M– ja G2-faasides ja kõige vastupidavamad hilises S-faasis. Pikema rakutsükli kestusega rakkudes on ka teine vastupidavuse kõrgpunkt, see on hilises G1-faasis.
Kõige kiiremini (9–10 tunniga) rakutsüklit läbivad imetajarakud on sooleepiteeli rakud. Samas tüvirakud hiire nahas võivad jaguneda rohkem kui 200 tunni tagant. Enamik rakutsükli pikkuse erinevustest on põhjustatud G1-faasi kestuse varieeruvusest. M- ja S-faasid nii palju ei varieeru.
Viited muuda
- ↑ Lodish, H. Molecular Cell Biology 5th edition, W. H. Freeman and Company, 2003
- ↑ Maton, Anthea; Hopkins, Jean Johnson, Susan LaHart, David, Quon Warner, David, Wright, Jill D (1997). Cells: Building Blocks of Life. New Jersey: Prentice Hall. pp. 70–4.
- ↑ Lilly M, Duronio R (2005). "New insights into cell cycle control from the Drosophila endocycle". Oncogene 24 (17): 2765–75.
- ↑ De Souza CP, Osmani SA (2007). "Mitosis, not just open or closed". Eukaryotic Cell 6 (9): 1521–7.
- ↑ Nigg EA (June 1995). "Cyclin-dependent protein kinases: key regulators of the eukaryotic cell cycle". Bioessays 17 (6): 471–80.
- ↑ "The Nobel Prize in Physiology or Medicine 2001"
- ↑ Stephen J. Elledge (6 December 1996). "Cell Cycle Checkpoints: Preventing an Identity Crisis" Science 274 (5293): 1664–1672.
- ↑ Robbins and Cotran; Kumar, Abbas, Fausto (2004). Pathological Basis of Disease. Elsevier.
Välislingid muuda
| Pildid, videod ja helifailid Commonsis: Rakutsükkel |
- Rakutsükkel. Mitoos.
- Katrin Kestav: "Võtame luubi alla rakujagunemise kontrollmehhanismid" ERR Novaator, 1. august 2016