Dessi-Martini perjodinaan
See artikkel ootab keeletoimetamist. |
Artikkel vajab vormindamist vastavalt Vikipeedia vormistusreeglitele. |
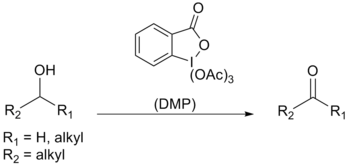
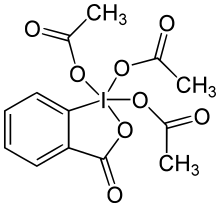
Dess-Martin perjodinaan (DMP), 1,1,1-triatsetoksü-1,1-dihüdro-1,2-dibensjodoksool-3(1H)-oon on organojoodne keemiline reagent, mida kasutatakse hõlpsaks ja tõhusaks primaarsete alkoholide aldehüüdideks ja sekundaarsete alkoholide ketoonideks oksüdeerimiseks.[1][2] Periodiaanil on palju eeliseid, vältides mõningaid tavapäraseid raskusi, mis esinevad teiste kroomi- ja DMSO-baasil toimuvatel oksüdatsiooniprotsessidel, näiteks nagu pikk ettevalmistus- ja reaktsiooniaeg või vajadus kasutada suurt kogust oksüdeerivat ainet, mis takistab DMP kasutamist kaubanduslikult, kuna DMP-l on kalduvus isoleerituna kuumutamisel tugevasti plahvatada. Heaks eelisteks teiste oksüdatsiooniprotsesside ees on neutraalne keskkond, toatemperatuur, kõrge kemoselektiivsus, hea tundlikkus mitmete funktsionaalrühmade suhtes ja pikk säilivusaeg. DMP-l on kõrge kuumatundlikkus ja löögitundlikkus. Ta on oma nime saanud Ameerika keemikute Daniel Benjamin Dessi ja James Cullen Martini järgi, kes töötasid välja reagendi 1983. aastal. Reagent baseerub ainel 1-hüdroksü-1,2-bensiodoksool-3(1H)-oon-1-oksiid) ehk 2-jodobensoehape (IBX), aga DMP on reaktiivsem ja lahustub palju paremini orgaanilistes solventides kui IBX, sest atsetaatrühmad on seotud tsentraalse ioodiaatomiga.[3]
Ettevalmistus muuda
Kõige lihtsamaks IBX sünteesiks loetakse 2-jodobensoehappe reageerimist oksooniga vesikeskkonnas kõrgendatud temperatuuril 3 tunni jooksul.[4] Seejärel IBX atsüleeritakse, kasutades Irelandi ja Liu modifikatsioone IBX originaalsünteesiprotseduurist.[5] Saadud tahkised filtritakse ja pestakse eetriga, Irelandi ja Liu meetodiga, kasutades katalüsaatorina tosüülhapet, mis kiirendab kogu reaktsiooni 2 tunnini (võrreldes tavasünteesiga, mis kestab ööpäeva) ja suurendades saagist 90%-ni.
Klassikaline meetod töötati välja Robert Boeckmani ja Joseph Mullinsi poolt.[6] Kaaliumbromiid, vesiniksulfaat ja 2-jodobensoehappe segu kuumutatakse, et saada IBX. Seejärel IBX atsüleeritakse atsetaathappe ja happe anhüdriidiga.
Plumb ja Harper avastasid, et mõlema oksüdeerija, IBX ja DMP, reaktsioon oli väga äkiline, tõestades nende plahvatusohtlikkust.[7]
Oksüdatsioonimehhanism muuda
Dess-Martin periodinaani kasutatakse põhiliselt oksüdeerijana kõrge tundlikkusega ja mitmeotstarbeliste alkoholidega. Üheks DMP efektiivsuse põhjusteks on tema kõrge selektiivsus antud alkoholi hüdroksüülrühma suhtes, mis põhjustab reaktsiooni esimeses etapis ligandi vahetuse. Prooton tuumamagnetresonantsspektroskoop(NMR) on tuvastanud, et kasutades ühte ekvivalenti alkoholi, tekib vaheproduktina diatsetoksüalkoksüperiodiaan. Seejärel atsetaat käitub reaktsioonis alusena, deprotoneerides α-H alkoholist, et tekiksid saadustena karbonüülne ühend, iodiaan ja atsetaathape. Kui kasutada diooli või rohkem kui üks ekvivalent alkoholi, tekib vaheühendina atsetoksüdialkoksüperiodiaan. Tänu vastava periodiaani labiilsele iseloomule toimub oksüdatsioon palju kiiremini.
Schreiber ja tema kaastöötajad on näidanud, et vesikeskkond aeglustab oksüdatsiooniprotsessi.[8] Dess ja Martin olid algselt uurinud, et etanooli oksüdatsiooniprotsess oli aeglasem, kui reaktsiooni oli lisatud ekstra ekvivalent etanooli. Eeldatakse, et hüdroksüülrühma võime loovutada elektrone(I-OAc sideme nõrgenemise tõttu) vähendab lõpp-produktis atsetaadi ligandi dissotsiatsiooni iodiinist.
Kemoselektiivsus muuda
Kasutades standardseid Dess-Martin periodinaani oksüdatsiooni tingimusi, saab alkohole oksüdeerida ketoonideks või aldehüüdideks ilma furaaniringe, sulfide, vinüüleetreid või sekundaarseid amiide mõjutamata. Allüülne alcohol, mis üldiselt raskesti oksüdeeritav vastavaks aldehüüdiks, on lihtsasti oksüdeeritavad kasutades DMP reagenti.[9] Myers ja tema kaastöötajad kinnitasid, et DMP võib oksüdeerida N-kaitstud-aminohappeid ilma epimeriseerimiseta (erinevalt teistest oksüdeerijatest, sealhulgas ka Swerni oksüdatsioonis). Need kaitstud aminohapped on väga olulised ravimitööstuses. Bensoe- ja allüülhapete reaktsioonid kulgevad kiiremini kui küllastunud alkoholid, sest DMP oksüdeerib aldoksiimid ja ketoksiimid nendele vastavateks aldehüüdideks ja ketoonideks kiiremini kui primaarset, sekundaarset või bensoealkoholi vastavaks karbonüülühendiks. [10]
Ühes Dess-Martini oksüdatsiooni näites toimub tundliku α-β-küllastamata alkoholi vahetus temale vastava aldehüüdiga. See molekuliosa on leitav mitmetes naturaalsetes produktides. Tema kõrge funktsionaalsuse tõttu on ta väärtuslik lisand paljudes orgaanilistes sünteesiprotseduurides. Thongsornkleeb ja Danheiser oksüdeerisid seda tundlikku alkoholi, kasutades töös Dess-Martini reagenti, muutes veidi tema sünteesiprotseduuri (lahjendamine pentaanidega, pesemine polü(4-vinüül)püridiiniga), et eemaldada äädikhape, mis tekib reaktsiooni käigus ja destilleerimise abil aine filtreeriti ja kontsentreeriti. [11]
t-butüül DMP muuda
Difluoro ja monofloro alkoholide oksüdeerimine on palju keerulisem. Nende oksüdeerimiseks on kasutatud Swerni oksüdatsiooni, kuid selle kindla oksüdatsiooniprotsessi käigus kasutatakse ära väga suur kogus oksüdeerijat. Mõningatel juhtudel ei saadud Swerni oksüdatsiooni käigus kätte isegi reprodutseeritavaid sünteesiprodukte. Linderman ja Graves leidsid, et DMP abil alkoholide sünteesimine on osaliselt tulus, omades mõningaid kõrvalreaktsioone. Kasutades modifitseeritud DMP oksüdeerijat, mis on näidatud allpool, produtseeriti soovitud karbonüülne ühend kõrge saagisega. Linderman ja Graves kasutasid alkoholi sünteesil ligandina tert-butüülalkoholi atsetaadi asemel, sest atsetaat ligandina on tuntud oma mitteoksüdatiivsete omaduste poolest. [12]
Viited muuda
- ↑ Dess, D. B.; Martin, J. C. "Readily accessible 12-I-5 oxidant for the conversion of primary and secondary alcohols to aldehydes and ketones" 1983 lk 48
- ↑ Boeckman, R.J.In "Encyclopedia of Reagents for Organic Synthesis" 1995 lk 1482
- ↑ Dess, D. B.; Martin, J. C. "Readily accessible 12-I-5 oxidant for the conversion of primary and secondary alcohols to aldehydes and ketones" 1983 lk 50
- ↑ Dess, D. B.; Martin, J. C. "A useful 12-I-5 triacetoxyperiodinane (the Dess-Martin periodinane) for the selective oxidation of primary or secondary alcohols and a variety of related 12-I-5 species" Kasutatud 03.11.2015
- ↑ Robert E. Ireland, Longbin Liu "An improved procedure for the preparation of the Dess-Martin periodinane" Kasutatud 03.11.2015
- ↑ "THE DESS-MARTIN PERIODINANE" Kasutatud 03.11.2015
- ↑ "Chemical Safety: 2-Iodoxybenzoic acid" Kasutatud 03.11.2015
- ↑ Stephanie D. Meyer, Stuart L. Schreiber"Acceleration of the Dess-Martin Oxidation by Water" Kasutatud 03.11.2015
- ↑ Nicholas J Lawrencea, J.Paul Crumpb, Alan T McGownb, John A Hadfieldb "Reaction of Baylis-Hillman products with Swern and Dess-Martin oxidants" Kasutatud 03.11.2015
- ↑ Andrew G Myers, Boyu Zhong, Mohammad Movassaghi, Daniel W Kung, Brian A Lanman, Soojin Kwon "Synthesis of highly epimerizable N-protected _-amino aldehydes of high enantiomeric excess" Kasutatud 03.11.2015
- ↑ Charnsak Thongsornkleeb, Rick L. Danheiser "A Practical Method for the Synthesis of 2-Alkynylpropenals" Kasutatud 23.11.2015
- ↑ Russell J. Linderman, David M. Graves "Oxidation of fluoroalkyl-substituted carbinols by the Dess-Martin reagent" Kasutatud 23.11.2015